Водоподготовка, хранение и продувка паровых котлов
Обзор химии воды, включая жёсткость и значения pH.
Прежде чем обсуждать и понимать продувку котла, необходимо определить, что такое вода, какие примеси она содержит, и связанные с этим понятия, такие как жёсткость, pH и т. д.
Вода — важнейшее сырьё на Земле. Она необходима для жизни, используется для транспортировки и служит накопителем энергии. Её также называют «универсальным растворителем».
Чистая вода (H20) в чистом состоянии не имеет вкуса, запаха и цвета; однако в природе полностью чистая вода встречается крайне редко. Все природные воды содержат различные виды и количества примесей.
Хорошая питьевая вода не обязательно является хорошей питательной водой для котла. Минералы в питьевой воде легко усваиваются человеческим организмом и важны для нашего благополучия. Котлы, напротив, справляются с ними гораздо хуже, и те же самые минералы могут повредить паровой котёл, если их не удалить.
Из мировых запасов воды 97% находится в океанах, а значительная часть остального заключена в полярных ледниках — для бытового и промышленного использования доступно только 0.65%.
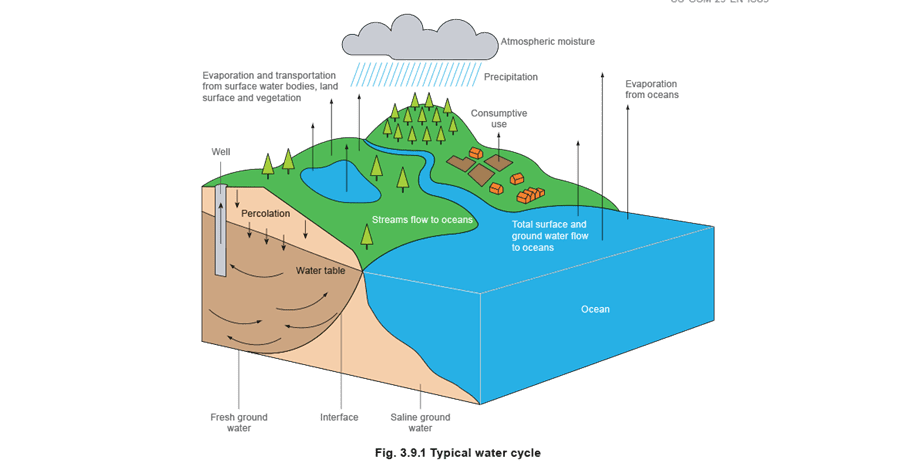
Эта небольшая доля была бы быстро исчерпана, если бы не круговорот воды в природе (см. Рисунок 3.9.1). После испарения вода превращается в облака, частично конденсируется во время перемещения и затем выпадает на землю в виде дождя. Однако неверно считать дождевую воду чистой: по пути к земле она поглощает такие примеси, как угольная кислота, азот и, в промышленных районах, диоксид серы.
С этими компонентами вода просачивается через верхние слои почвы к водоносному горизонту или течёт по поверхности земли, растворяя и собирая дополнительные примеси.
Эти примеси могут образовывать отложения на поверхностях теплопередачи, которые могут:
- вызывать коррозию металла;
- снижать интенсивность теплопередачи, приводя к перегреву и потере механической прочности.
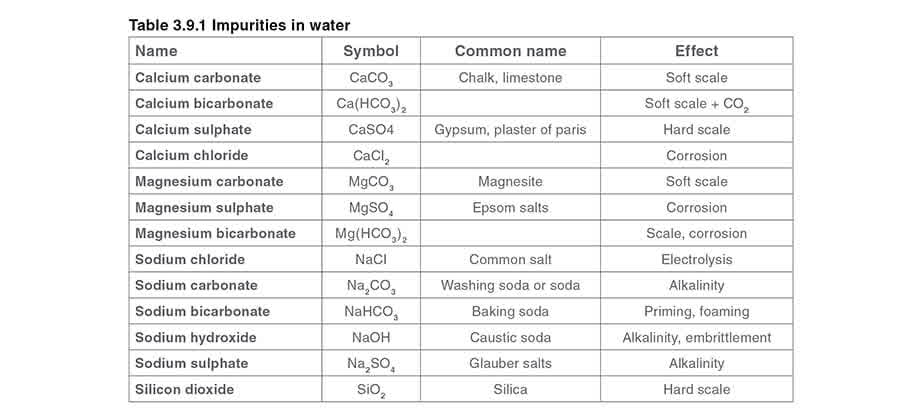
Таблица 3.9.1 показывает технические и общеупотребительные названия примесей, их химические обозначения и вызываемые ими эффекты.
Качество исходной воды и региональные различия
Качество исходной воды и региональные различия
Качество воды может сильно различаться от региона к региону в зависимости от источников воды и местных минералов (см. Рисунок 3.9.2). Таблица 3.9.2 приводит типичные значения для различных районов даже в такой относительно небольшой стране, как Великобритания.
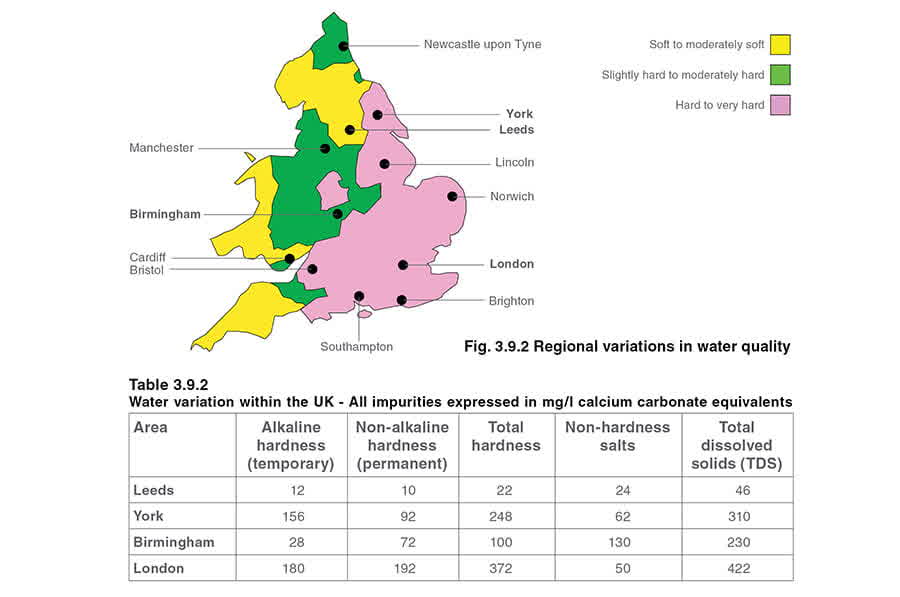 Распространённые примеси в исходной воде можно классифицировать следующим образом:
Распространённые примеси в исходной воде можно классифицировать следующим образом:
- Растворённые вещества — вещества, растворяющиеся в воде. Основные из них — карбонаты и сульфаты кальция и магния, которые при нагреве образуют накипь. Существуют и другие растворённые вещества, не образующие накипи. На практике любые соли, образующие накипь в котле, следует химически преобразовывать так, чтобы они образовывали взвешенные вещества или шлам, а не накипь.
- Взвешенные вещества — вещества, находящиеся в воде в виде взвешенных частиц. Обычно они имеют минеральное или органическое происхождение. Как правило, такие вещества не создают проблемы, поскольку могут быть отфильтрованы.
- Растворённые газы — кислород и углекислый газ легко растворяются в воде. Эти газы активно вызывают коррозию.
- Вспенивающие вещества — минеральные примеси, вызывающие вспенивание или образование поверхностной плёнки. Один из примеров — сода в форме карбоната, хлорида или сульфата.
Количество примесей крайне мало, и в анализах воды его обычно выражают в ppm по массе или, альтернативно, в mg/l.
Следующие разделы этого модуля описывают свойства воды.
Жёсткость
Жёсткость
Воду называют либо «жёсткой», либо «мягкой». Жёсткая вода содержит примеси, образующие накипь, тогда как мягкая вода содержит их мало или не содержит вовсе. Разницу легко определить по воздействию воды на мыло: для образования пены в жёсткой воде требуется гораздо больше мыла, чем в мягкой.
Жёсткость вызывается присутствием минеральных солей кальция и магния, и именно эти минералы способствуют образованию накипи.
Существуют две распространённые классификации жёсткости:
- Щёлочная жёсткость (также называемая временной жёсткостью) — бикарбонаты кальция и магния отвечают за щёлочную жёсткость. Эти соли растворяются в воде, образуя щелочной раствор. При нагревании они разлагаются с выделением углекислого газа и образованием мягкой накипи или шлама.
Термин «временная жёсткость» иногда используется потому, что такая жёсткость удаляется кипячением.
Это явление часто можно наблюдать в виде накипи внутри электрического чайника.
См. Рисунки 3.9.3 и 3.9.4 — последний из них показывает ситуацию внутри котла.
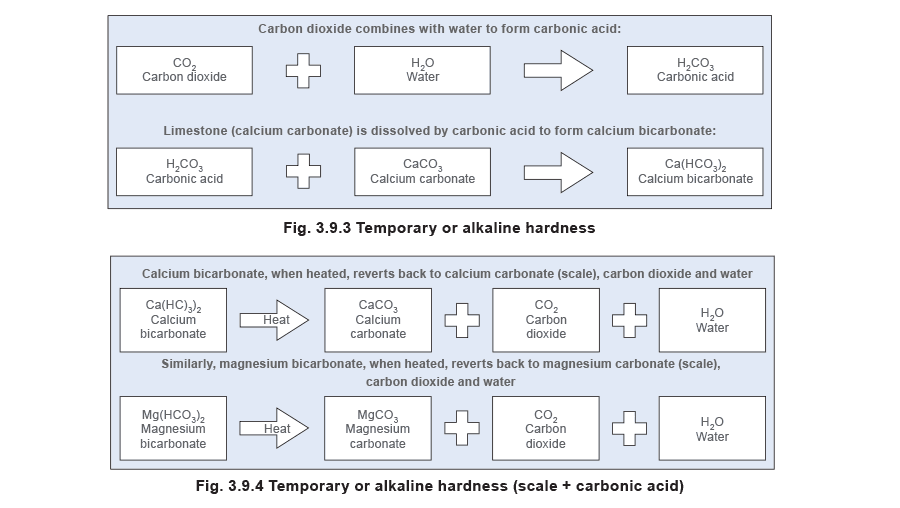
- Нещёлочная жёсткость (также называемая постоянной жёсткостью) — также вызвана наличием солей кальция и магния, но в форме сульфатов и хлоридов. Из-за уменьшения растворимости при повышении температуры они выпадают из раствора и образуют твёрдую накипь, которую трудно удалять.
Кроме того, присутствие кремнезёма в котловой воде также может приводить к образованию твёрдой накипи, которая может взаимодействовать с солями кальция и магния с образованием силикатов, серьёзно ухудшающих теплопередачу через жаровые трубы и вызывающих их перегрев.
Общая жёсткость
Общая жёсткость
Общая жёсткость не классифицируется как отдельный тип жёсткости, а представляет собой сумму концентраций ионов кальция и магния, если обе выражены как CaC03. Если вода щёлочная, часть этой жёсткости, равная по величине общей щёлочности и также выраженная как CaC03, считается щёлочной жёсткостью, а остаток — нещелочной жёсткостью (см. Рисунок 3.9.5).

Соли, не образующие накипь
Соли, не образующие накипь
Соли, не относящиеся к солям жёсткости, например соли натрия, также присутствуют в воде. Они гораздо более растворимы, чем соли кальция или магния, и обычно не образуют накипи на поверхностях котла, как показано на Рисунке 3.9.6.
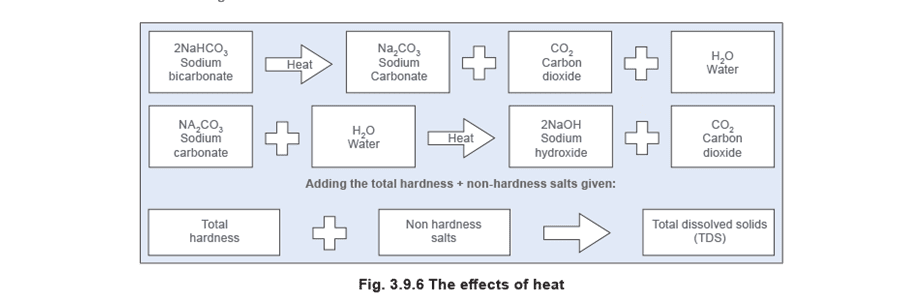 Сравнительные единицы
Сравнительные единицы
Когда соли растворяются в воде, они образуют электрически заряженные частицы, называемые ионами.
Металлические компоненты (кальций, натрий, магний) идентифицируются как катионы, потому что они притягиваются к катоду и несут положительный электрический заряд.
Анионы неметаллические и несут отрицательный заряд — бикарбонаты, карбонаты, хлориды и сульфаты притягиваются к аноду.
Каждая примесь обычно выражается как химически эквивалентное количество карбоната кальция, молекулярная масса которого равна 100.
Значение pH
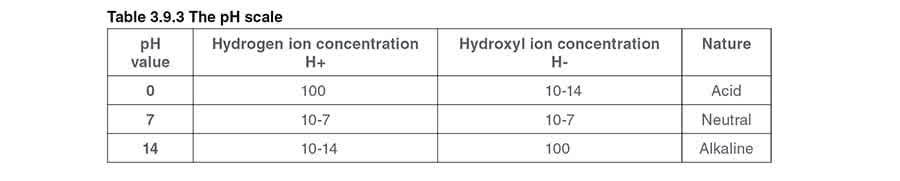
Ещё один важный термин — значение pH; это не примесь и не компонент, а числовая величина, характеризующая потенциальное содержание водорода в воде, то есть степень её кислотности или щёлочности. Вода H2O содержит два типа ионов — ионы водорода (H+) и гидроксильные ионы (OH-).
Если преобладают ионы водорода, раствор будет кислым, со значением pH от 0 до 6. Если преобладают гидроксильные ионы, раствор будет щелочным, со значением pH от 8 до 14. Если количество водородных и гидроксильных ионов одинаково, раствор нейтрален, и его pH равен 7. Кислоты и щёлочи увеличивают электропроводность воды по сравнению с нейтральным образцом. Например, образец воды с pH 12 будет иметь более высокую электропроводность, чем образец с pH 7.
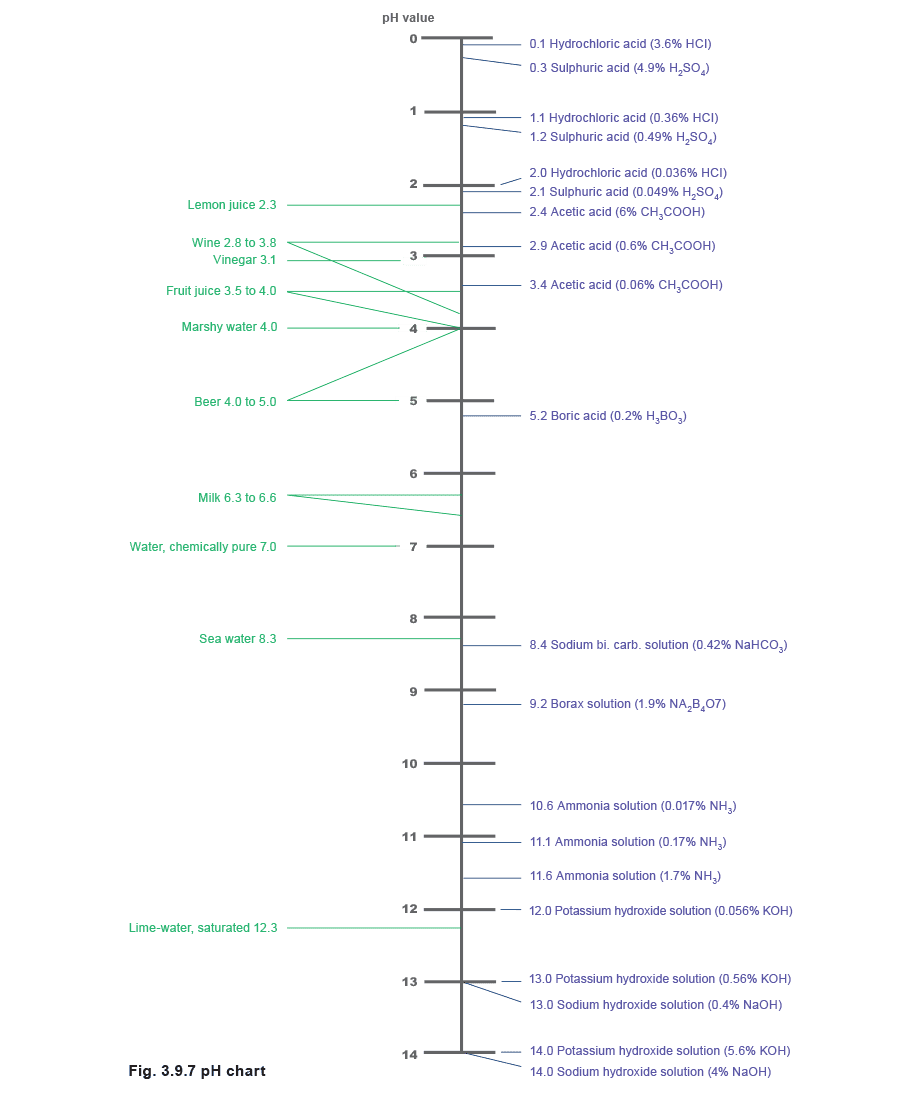
Таблица 3.9.3 показывает шкалу pH, а Рисунок 3.9.7 иллюстрирует уже упомянутые значения pH как численно, так и по отношению к повседневным веществам.