Что такое пар?
Здесь рассматриваются свойства пара, включая способность пара под давлением переносить, а затем отдавать большие количества энергии. Темы включают таблицы насыщенного пара, степень сухости и flash steam.
Лучше понять свойства пара можно, если сначала понять общую молекулярную и атомную структуру вещества, а затем применить это знание к льду, воде и пару.
Молекула - это наименьшее количество любого элемента или химического соединения, которое еще сохраняет все химические свойства этого вещества и может существовать самостоятельно. Сами молекулы состоят из еще более мелких частиц, называемых атомами, которые определяют базовые элементы, такие как водород и кислород.
Определенные комбинации этих атомных элементов образуют химические соединения. Одно из таких соединений описывается химической формулой H2O и состоит из молекул, содержащих два атома водорода и один атом кислорода.
Причина того, что вода столь распространена на Земле, состоит в том, что водород и кислород являются одними из самых распространенных элементов во Вселенной. Углерод - еще один весьма распространенный элемент и ключевая составляющая всей органической материи.
Большинство минеральных веществ могут существовать в трех физических состояниях, твердо́м, жидком и парообразном, которые называют фазами. В случае H2O эти три фазы соответственно обозначаются как лед, вода и пар.
Молекулярное строение льда, воды и пара до конца еще не изучено, однако удобно считать, что молекулы связаны друг с другом электрическими зарядами, называемыми водородной связью. Степень возбуждения молекул определяет физическое состояние, или фазу, вещества.
Тройная точка
Все три фазы конкретного вещества могут сосуществовать в равновесии только при определенных температуре и давлении; это состояние называется тройной точкой.
Тройная точка H2O, при которой лед, вода и пар находятся в равновесии, соответствует температуре 273,16 K и абсолютному давлению 0,006 112 бар. Это давление очень близко к идеальному вакууму. Если при этой температуре давление понизить еще сильнее, лед вместо плавления будет сублимировать непосредственно в пар.
Лед
Лед
Во льду молекулы жестко зафиксированы в упорядоченной решетчатой структуре и могут только вибрировать.
В твердой фазе движение молекул в решетке представляет собой колебания около среднего связанного положения, где расстояние между молекулами меньше одного молекулярного диаметра.
Непрерывное подведение теплоты увеличивает амплитуду колебаний до такой степени, что некоторые молекулы в конечном итоге отрываются от соседних, и твердое тело начинает плавиться, переходя в жидкое состояние. При атмосферном давлении плавление происходит при 0 °C. Изменения давления очень слабо влияют на температуру плавления, поэтому для большинства практических целей 0 °C можно принимать как точку плавления. Однако известно, что температура плавления льда уменьшается на 0,0072 °C на каждую дополнительную атмосферу давления. Например, давление 13,9 бар изб. потребовалось бы, чтобы снизить температуру плавления на 0,1 °C.
Теплота, которая разрушает связи в кристаллической решетке и вызывает фазовый переход без повышения температуры льда, называется энтальпией плавления или теплотой плавления. Это явление фазового перехода обратимо: при замерзании то же количество теплоты выделяется обратно в окружающую среду.
Для большинства веществ плотность уменьшается при переходе из твердой фазы в жидкую.
Однако H2O является исключением из этого правила, поскольку при плавлении его плотность возрастает, и именно поэтому лед плавает на воде.
Вода
Вода
В жидкой фазе молекулы могут свободно перемещаться, но по-прежнему находятся на расстоянии меньше одного молекулярного диаметра из-за взаимного притяжения, и столкновения происходят часто. Дополнительная теплота усиливает молекулярное движение и столкновения, повышая температуру жидкости вплоть до температуры кипения.
Энтальпия воды, жидкостная энтальпия или чувствительная теплота воды, hf
Это количество тепловой энергии, необходимое для повышения температуры воды от исходной точки 0 °C до ее текущей температуры.
В этом опорном состоянии, при 0 °C, энтальпия воды условно принята равной нулю. Тогда энтальпию всех остальных состояний можно определять относительно этой легко доступной базовой точки.
Термин sensible heat использовался раньше, поскольку добавление теплоты к воде вызывало изменение температуры. Однако принятыми терминами сегодня являются liquid enthalpy или enthalpy of water.
При атмосферном давлении, 0 бар изб., вода кипит при 100 °C, и для нагрева 1 кг воды от 0 °C до температуры кипения 100 °C требуется 419 кДж энергии. Именно на основе этих значений для большинства расчетов в диапазоне от 0 °C до 100 °C получают величину удельной теплоемкости воды Cp = 4,19 кДж/кг °C.
Пар
Пар
По мере роста температуры и приближения воды к кипению некоторые молекулы приобретают достаточно кинетической энергии, чтобы достичь скоростей, позволяющих им на короткое время покинуть жидкость и перейти в пространство над ее поверхностью, прежде чем снова упасть обратно в жидкость. Дальнейший нагрев приводит к большему возбуждению, и число молекул, обладающих достаточной энергией для выхода из жидкости, увеличивается. Когда вода нагревается до точки кипения, внутри нее формируются пузырьки пара, которые поднимаются и прорываются через поверхность. Если рассматривать молекулярную структуру жидкостей и паров, логично, что плотность пара намного меньше плотности воды, поскольку молекулы пара находятся дальше друг от друга. Поэтому пространство непосредственно над поверхностью воды заполняется менее плотными молекулами пара. Когда число молекул, покидающих поверхность жидкости, становится больше числа возвращающихся обратно, вода свободно испаряется. В этот момент она достигает точки кипения, или температуры насыщения, поскольку насыщена тепловой энергией. Если давление остается постоянным, добавление дальнейшей теплоты уже не вызывает повышения температуры, а приводит к образованию насыщенного пара. Температура кипящей воды и насыщенного пара в пределах одной и той же системы одинакова, но тепловая энергия на единицу массы в паре значительно выше. При атмосферном давлении температура насыщения равна 100 °C. Однако если давление увеличить, это позволит подвести больше теплоты и повысить температуру без фазового перехода. Следовательно, увеличение давления фактически увеличивает как энтальпию воды, так и температуру насыщения. Связь между температурой насыщения и давлением известна как кривая насыщения пара, см. рисунок 2.2.1.
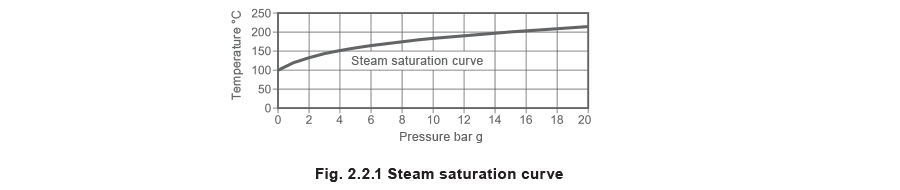
Вода и пар могут сосуществовать при любом давлении на этой кривой, причем оба находятся при температуре насыщения. Пар в состоянии выше кривой насыщения называется перегретым паром:
- температура выше температуры насыщения называется степенью перегрева пара;
- вода в состоянии ниже кривой называется недонасыщенной водой.
Если пар может выходить из котла с той же скоростью, с какой он образуется, то дальнейшее подведение теплоты просто увеличивает скорость образования пара. Если же пару не дают выходить из котла, а скорость подвода теплоты сохраняется, то поток энергии, входящий в котел, будет больше потока энергии, выходящего из него. Избыточная энергия повышает давление, а это, в свою очередь, позволяет температуре насыщения расти, поскольку температура насыщенного пара связана с его давлением.
Энтальпия испарения, или скрытая теплота,
hfgЭто количество теплоты, необходимое для перевода воды при ее температуре кипения в пар. При этом температура пароводяной смеси не изменяется, и вся энергия используется для фазового перехода из жидкости, воды, в пар, насыщенный пар. Старый термин latent heat основан на том, что теплота подводилась, но температура не менялась. Однако принятым термином теперь является enthalpy of evaporation. Как и переход из льда в воду, процесс испарения также обратим. То же количество теплоты, которое образовало пар, выделяется обратно в окружающую среду при конденсации, когда пар встречается с поверхностью, имеющей более низкую температуру. Эту часть можно считать полезной составляющей теплоты в паре для целей нагрева, поскольку именно она извлекается, когда пар конденсируется обратно в воду. Энтальпия насыщенного пара, или полная теплота насыщенного пара Это полная энергия насыщенного пара, и она равна сумме энтальпии воды и энтальпии испарения.

Энтальпию, как и другие свойства насыщенного пара, можно легко определить по табличным результатам предыдущих экспериментов, известным как паровые таблицы.
Таблицы насыщенного пара
В паровых таблицах перечислены свойства пара при различных давлениях. Это результаты реальных испытаний, проведенных с паром. Таблица 2.2.1 показывает свойства сухого насыщенного пара при атмосферном давлении, 0 бар изб.
Таблица 2.2.1 Свойства насыщенного пара при атмосферном давлении
| Удельная энтальпия, энергия, кДж/кг | |||||
| Давление, бар изб. | Температура насыщения, °C | Вода, hf | Испарение, hfg | Пар, hg | Удельный объем сухого насыщенного пара, м3/кг |
| 0 | 100 | 419 | 2 257 | 2 676 | 1.673 |
Пример 2.2.1
Пример 2.2.1
При атмосферном давлении, 0 бар изб., вода кипит при 100 °C, и для нагрева 1 кг воды от 0 °C до температуры насыщения 100 °C требуется 419 кДж энергии. Следовательно, удельная энтальпия воды при 0 бар изб. и 100 °C составляет 419 кДж/кг, как показано в паровых таблицах, см. таблицу 2.2.2.
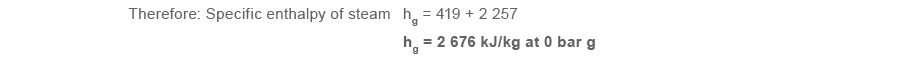
Однако пар при атмосферном давлении имеет ограниченную практическую ценность. Это связано с тем, что он не может транспортироваться по паропроводу к точке использования только за счет собственного давления.
Примечание: из-за зависимости давления и объема пара, объем уменьшается при увеличении давления, пар обычно вырабатывается в котле при давлении не менее 7 бар изб. Получение пара при более высоких давлениях позволяет сохранять парораспределительные трубопроводы разумного диаметра. По мере роста давления пара его плотность также увеличивается. Поскольку удельный объем обратно пропорционален плотности, удельный объем уменьшается с увеличением давления. На рисунке 2.2.2 показана зависимость удельного объема от давления. Из него видно, что наибольшее изменение удельного объема происходит при низких давлениях, тогда как в верхней части диапазона изменения значительно меньше.
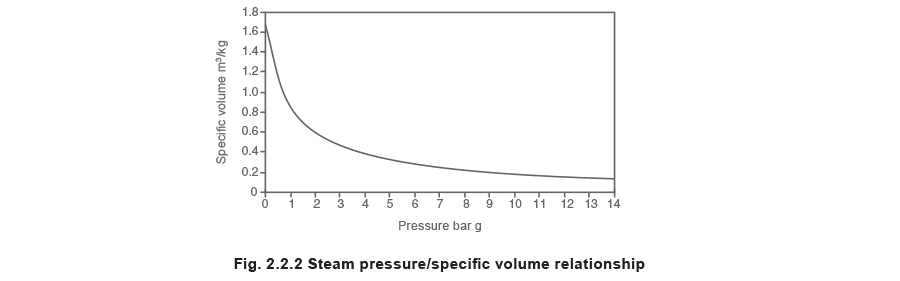
Фрагмент паровых таблиц, показанный в таблице 2.2.2, содержит удельный объем и другие данные, относящиеся к насыщенному пару.
При 7 бар изб. температура насыщения воды составляет 170 °C. Для нагрева воды до точки насыщения при 7 бар изб. требуется больше тепловой энергии, чем было бы нужно при атмосферном давлении. Таблица дает значение 721 кДж для нагрева 1 кг воды от 0 °C до температуры насыщения 170 °C. Тепловая энергия, энтальпия испарения, необходимая воде при 7 бар изб. для превращения в пар, на самом деле меньше, чем при атмосферном давлении. Это связано с тем, что удельная энтальпия испарения уменьшается с ростом давления пара. Однако поскольку удельный объем также уменьшается с увеличением давления, количество передаваемой тепловой энергии в одном и том же объеме в действительности возрастает с ростом давления пара.
Таблица 2.2.2 Фрагмент таблицы насыщенного пара
| Давление, бар изб. | Температура насыщения, °C | Удельная энтальпия, энергия, кДж/кг | Удельный объем сухого насыщенного пара, м3/кг | ||
| Вода, hf | Испарение, hfg | Пар, hg | |||
| 0 | 100 | 419 | 2 257 | 2 676 | 1.673 |
| 1 | 120 | 506 | 2 201 | 2 707 | 0.881 |
| 2 | 134 | 562 | 2 163 | 2 725 | 0.603 |
| 3 | 144 | 605 | 2 133 | 2 738 | 0.461 |
| 4 | 152 | 641 | 2 108 | 2 749 | 0.374 |
| 5 | 159 | 671 | 2 086 | 2 757 | 0.315 |
| 6 | 165 | 697 | 2 066 | 2 763 | 0.272 |
| 7 | 170 | 721 | 2 048 | 2 769 | 0.240 |
Степень сухости
Пар с температурой, равной температуре кипения при данном давлении, называется сухим насыщенным паром. Однако в промышленном котле, рассчитанном на выработку насыщенного пара, получить 100% сухой пар удается редко, и обычно пар содержит капли воды.
На практике из-за турбулентности и разбрызгивания, когда пузырьки пара прорываются через поверхность воды, паровое пространство содержит смесь капель воды и пара.
Пар, вырабатываемый в любом котле shell-type, см. раздел 3, где теплота подводится только к воде и где пар остается в контакте с поверхностью воды, может обычно содержать около 5% воды по массе.
Если содержание воды в паре составляет 5% по массе, то говорят, что пар имеет сухость 95% и степень сухости 0,95.
Фактическая энтальпия испарения влажного пара равна произведению степени сухости, c, и удельной энтальпии hfg из паровых таблиц. Влажный пар имеет меньшую полезную тепловую энергию, чем сухой насыщенный пар.
 Следовательно:
Следовательно:
 Поскольку удельный объем воды на несколько порядков меньше удельного объема пара, капли воды во влажном паре занимают пренебрежимо малый объем. Поэтому удельный объем влажного пара будет меньше, чем у сухого пара:
Поскольку удельный объем воды на несколько порядков меньше удельного объема пара, капли воды во влажном паре занимают пренебрежимо малый объем. Поэтому удельный объем влажного пара будет меньше, чем у сухого пара:
 Где
Где vg - удельный объем сухого насыщенного пара.
Пример 2.2.2
Пример 2.2.2
Пар при давлении 6 бар изб. и степени сухости 0,94 будет содержать только 94% энтальпии испарения сухого насыщенного пара при 6 бар изб. В приведенных ниже расчетах используются значения из паровых таблиц:

Фазовая диаграмма пара Данные, приведенные в паровых таблицах, можно также представить в графической форме. На рисунке 2.2.3 показана связь между энтальпией и температурой для различных состояний воды и пара; это называется фазовой диаграммой.
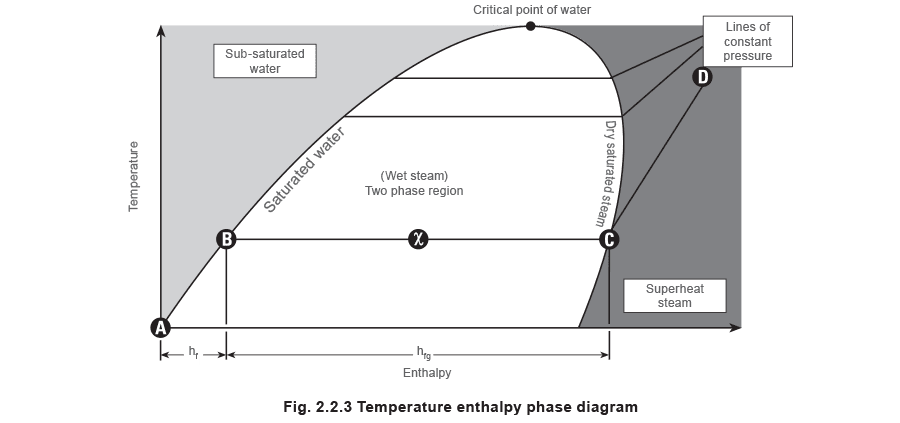
Когда вода нагревается от 0 °C до температуры насыщения, ее состояние следует по линии насыщенной воды, пока она не получит всю свою жидкостную энтальпию hf, участок A - B.
Если после этого продолжать подводить теплоту, вода меняет фазу и превращается в смесь воды и пара, при этом энтальпия продолжает расти, а температура остается равной температуре насыщения, hfg, участок B - C.
По мере увеличения сухости пароводяной смеси ее состояние смещается от линии насыщенной жидкости к линии насыщенного пара. Поэтому в точке, расположенной ровно посередине между этими двумя состояниями, степень сухости c равна 0,5. Аналогично на линии насыщенного пара пар имеет 100% сухость.
Когда пар получает всю свою энтальпию испарения, он достигает линии насыщенного пара. Если после этого нагрев продолжается, давление остается постоянным, но температура пара начинает повышаться за счет перегрева, участок C - D.
Линии насыщенной воды и насыщенного пара ограничивают область, в которой существует смесь воды и пара, то есть влажный пар. В области слева от линии насыщенной воды существует только вода, а в области справа от линии насыщенного пара существует только перегретый пар.
Точка, в которой линия насыщенной воды и линия насыщенного пара сходятся, называется критической точкой. По мере увеличения давления и приближения к критической точке энтальпия испарения уменьшается, пока не становится равной нулю в самой критической точке. Это означает, что в критической точке вода непосредственно переходит в насыщенный пар.
Выше критической точки пар можно рассматривать как газ. Газообразное состояние - это наиболее разреженное состояние, в котором молекулы имеют почти неограниченное движение, а объем увеличивается без предела при снижении давления.
Критическая точка - это наивысшая температура, при которой вода вообще может существовать. Любое сжатие при постоянной температуре выше критической точки не приведет к фазовому переходу.
Однако сжатие при постоянной температуре ниже критической точки приведет к сжижению пара, когда он будет переходить из области перегретого пара в область влажного пара.
Для пара критическая точка соответствует 374,15 °C и 221,2 бар абс. Выше этого давления пар называют сверхкритическим, и четко определенная точка кипения уже не существует.
Flash Steam
Термин flash steam традиционно используется для описания пара, выходящего из вентиляционных отверстий сборников конденсата и из открытых линий сброса конденсата после steam traps. Как может образоваться пар из воды без дополнительного подвода теплоты?
Flash steam возникает всякий раз, когда вода под высоким давлением, с температурой выше температуры насыщения жидкости при более низком давлении, попадает в область более низкого давления. И наоборот, если температура воды высокого давления ниже температуры насыщения при низком давлении, flash steam образоваться не может. В случае конденсата, проходящего через steam trap, температура на входе обычно достаточно высока для образования flash steam. См. рисунок 2.2.4.

Рассмотрим один килограмм конденсата при 5 бар изб. и температуре насыщения 159 °C, проходящий через steam trap к более низкому давлению 0 бар изб. Количество энергии в одном килограмме конденсата при температуре насыщения и давлении 5 бар изб. составляет 671 кДж. Согласно первому закону термодинамики, количество энергии, содержащейся в жидкости на стороне низкого давления после steam trap, должно быть равно количеству энергии на стороне высокого давления; это и составляет принцип сохранения энергии.
Следовательно, теплота, содержащаяся в одном килограмме жидкости низкого давления, также составляет 671 кДж. Однако вода при 0 бар изб. может содержать только 419 кДж теплоты, поэтому на стороне низкого давления возникает кажущийся избыток теплоты: 671 - 419 = 252 кДж, который можно считать избыточной теплотой.
Эта избыточная теплота вскипячивает часть конденсата и образует так называемый flash steam, а сам процесс кипения называется flashing. Следовательно, один килограмм конденсата, который существовал как один килограмм жидкой воды на стороне высокого давления steam trap, теперь на стороне низкого давления частично существует как вода и частично как пар.
Количество flash steam, образующегося при конечном давлении, P2, можно определить с помощью уравнения 2.2.5:

Пример 2.2.3
Пример 2.2.3
Случай, когда температура конденсата высокого давления выше температуры насыщения при низком давлении. Рассмотрим некоторое количество воды при давлении 5 бар изб., содержащее 671 кДж/кг тепловой энергии при температуре насыщения 159 °C. Если затем давление понизить до атмосферного, 0 бар изб., вода сможет существовать только при 100 °C и содержать 419 кДж/кг тепловой энергии. Эта разница, 671 - 419 = 252 кДж/кг тепловой энергии, и приведет к образованию flash steam при атмосферном давлении.
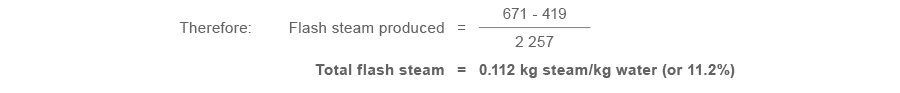
Долю образующегося flash steam можно представить как отношение избыточной энергии к энтальпии испарения при конечном давлении.
Пример 2.2.4
Пример 2.2.4
Случай, когда температура конденсата высокого давления ниже температуры насыщения при низком давлении. Рассмотрим те же условия, что и в примере 2.2.3, за исключением того, что температура конденсата высокого давления составляет 90 °C, то есть он доохлажден ниже атмосферной температуры насыщения 100 °C. Примечание: столь большое снижение температуры конденсата по сравнению с температурой насыщения, в данном случае с 159 °C до 90 °C, обычно непрактично; этот пример используется лишь для иллюстрации того, что при таких условиях flash steam не образуется. В этом случае таблица недонасыщенной воды покажет, что жидкостная энтальпия одного килограмма конденсата при 5 бар изб. и 90 °C составляет 377 кДж. Поскольку эта энтальпия меньше, чем энтальпия одного килограмма насыщенной воды при атмосферном давлении, 419 кДж, никакой избыточной теплоты для образования flash steam нет. Конденсат просто проходит через trap и остается в жидком состоянии при той же температуре, но уже при более низком давлении, в данном случае атмосферном. См. рисунок 2.2.5.

Давление насыщенного пара воды при 90 °C составляет 0,7 бар абсолютного. Если бы нижнее давление конденсата было меньше этого значения, flash steam образовался бы.
Принципы сохранения энергии и массы между двумя состояниями процесса
Принципы сохранения энергии и массы между двумя состояниями процесса
Принципы сохранения энергии и массы позволяют посмотреть на явление flash steam и с другой стороны.
Рассмотрим условия примера 2.2.3. 1 кг конденсата при 5 бар изб. и 159 °C образует 0,112 кг flash steam при атмосферном давлении. Это можно схематически показать на рисунке 2.2.6. Общая масса flash steam и конденсата остается равной 1 кг.
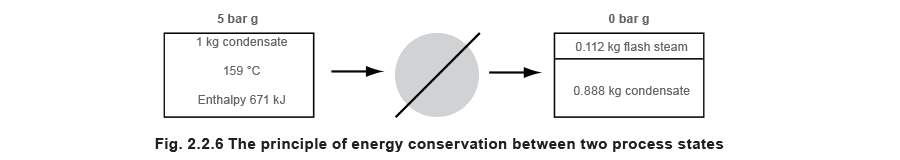
Принцип сохранения энергии гласит, что полная энергия в состоянии после понижения давления должна быть равна полной энергии в состоянии до понижения давления. Следовательно, количество теплоты в flash steam и конденсате должно быть равно количеству теплоты в исходном конденсате, то есть 671 кДж.
Паровые таблицы дают следующую информацию:

Следовательно, согласно паровым таблицам, энтальпия, ожидаемая в состоянии после понижения давления, совпадает с энтальпией в состоянии до понижения давления, что подтверждает принцип сохранения энергии.
