Энтропия - базовое понимание
Энтропия - понятие, которое некоторым кажется трудным для понимания, хотя в действительности оно не заслуживает такой репутации. Рассматривайте энтропию как дорожную карту, связывающую термодинамические состояния. Этот материал призван пролить свет на тему, подходя к ней с первых принципов.
Что такое энтропия?
Что такое энтропия?
В некотором смысле проще сказать, чем энтропия не является. Это не физическое свойство пара вроде давления, температуры или массы. Датчик не может ее измерить, и на манометре она не отображается. Ее нужно вычислять по величинам, которые можно измерить. Затем значения энтропии можно tabулировать и использовать в расчетах, особенно в расчетах течения пара и выработки мощности с помощью турбин или поршневых машин. В определенном смысле это мера недостатка качества или доступности энергии, а также того, как энергия всегда стремится распространяться от источника с высокой температурой к более широкой области с более низкой температурой. Именно это стремление к рассеиванию побудило некоторых наблюдателей назвать энтропию "стрелой времени". Если энтропия системы рассчитана для двух разных состояний, то состояние с большей энтропией соответствует более позднему моменту времени. Рост энтропии в общей системе всегда происходит в том же направлении, в котором течет время. Это может представлять философский интерес, но не слишком помогает при вычислении реальных значений. Более практично определять энтропию как энергию, подведенную к системе или отведенную от нее, деленную на среднюю абсолютную температуру, в диапазоне которой происходит изменение. Чтобы понять, как это работает, лучше всего начать с диаграммы, показывающей, как энтальпия одного килограмма воды увеличивается при нагреве до различных давлений и испарении в пар.
Поскольку температура и давление кипения воды жестко связаны между собой, рисунок 2.15.1 можно было бы также построить как график энтальпии от температуры, а затем повернуть так, чтобы температура стала вертикальной осью, а энтальпия - горизонтальной, как на рисунке 2.15.2.
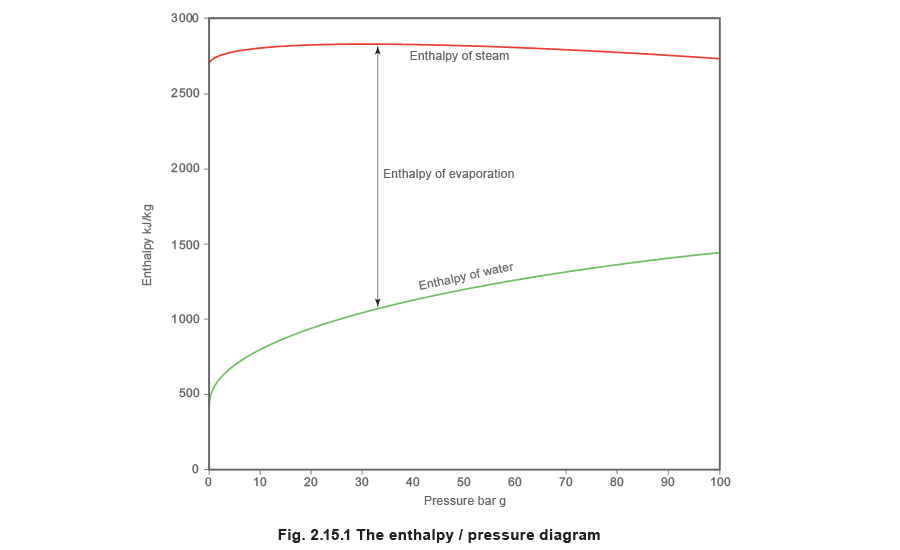
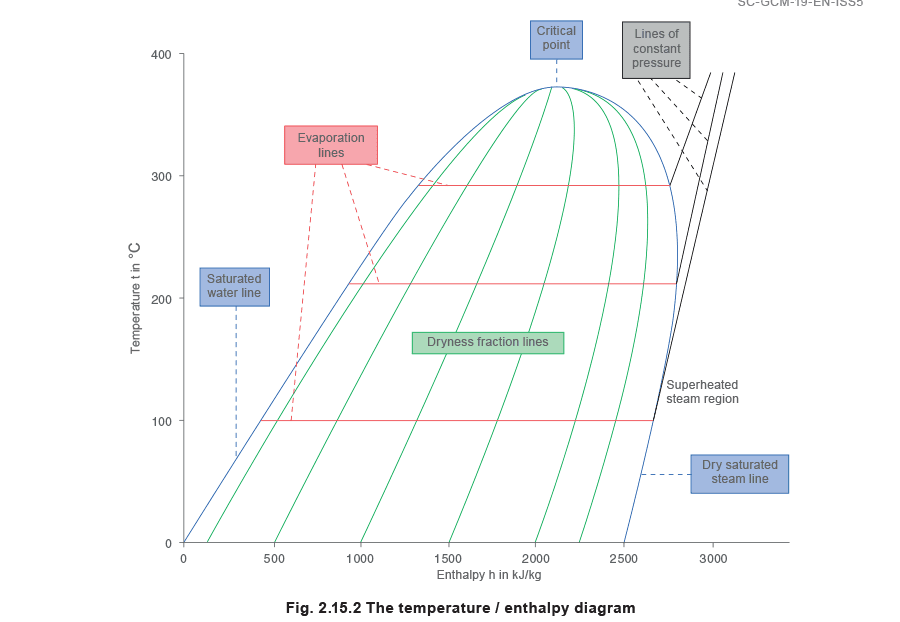
Линии постоянного давления начинаются на линии насыщенной воды. Горизонтальное расстояние между линией насыщенной воды и линией сухого насыщенного пара представляет собой количество скрытой теплоты или энтальпии испарения и называется линией испарения; при повышении давления энтальпия испарения уменьшается. Область справа от линии сухого насыщенного пара является областью перегретого пара, и линии постоянного давления начинают изгибаться вверх, как только пересекают линию сухого насыщенного пара.
Очень полезной разновидностью диаграммы на рисунке 2.15.2 является вариант, в котором по горизонтальной оси откладывается не энтальпия, а энтальпия, деленная на среднюю температуру, при которой энтальпия подводится или отводится. Для построения такой диаграммы можно рассчитать значения энтропии. Начиная от начала координат при температуре 0 °C и атмосферном давлении и добавляя энтальпию небольшими порциями, можно построить график. Поскольку энтропия измеряется относительно абсолютной температуры, начальная температура 0 °C принимается равной 273.15 K. Удельная теплоемкость насыщенной воды при этой температуре составляет 4.228 kJ/kg K. Для построения диаграммы на рисунке 2.15.3 базовая температура принимается равной 273 K, а не 273.15 K. Если взять один килограмм воды при атмосферном давлении и добавить 4.228 kJ энергии, температура воды повысится на 1 K - с 273 K до 274 K. Средняя температура в ходе этой операции составит 273.5 K, см. рисунок 2.15.3.
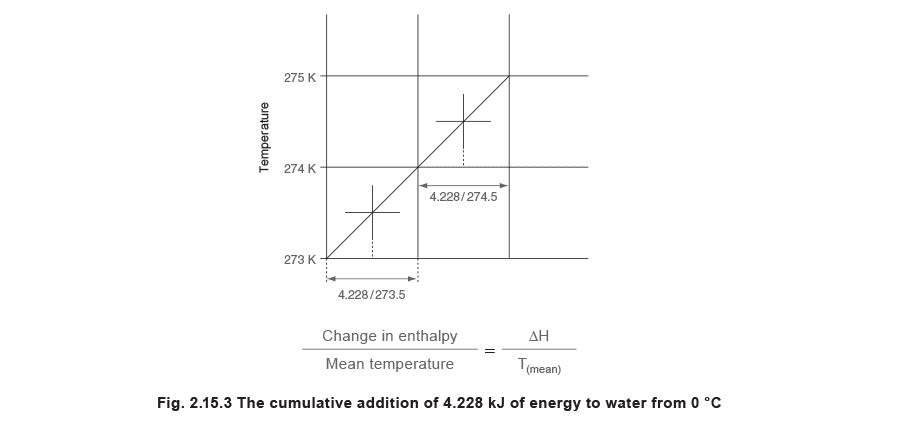
Это значение представляет изменение энтальпии на каждый градус повышения температуры для одного килограмма воды и называется изменением удельной энтропии. Следовательно, метрическими единицами удельной энтропии являются kJ/kg K.
Этот процесс можно продолжить, добавляя еще по 4.228 kJ энергии, чтобы получить ряд таких точек на линии состояния. На следующем шаге температура повысится с 274 K до 275 K, а средняя температура составит 274.5 K.

Из этих простых расчетов видно, что по мере роста температуры изменение энтропии на каждый одинаковый прирост энтальпии немного уменьшается. Если продолжать этот пошаговый процесс, добавляя все больше тепла, станет заметно, что изменение энтропии продолжает уменьшаться. Это происходит потому, что каждый дополнительный прирост тепла повышает температуру и тем самым уменьшает ширину соответствующей элементарной полосы. По мере дальнейшего подвода тепла линия состояния, в данном случае линия насыщенной воды, плавно изгибается вверх.
При 373.14 K (99.99 °C) при атмосферном давлении достигается точка кипения воды, и дальнейший подвод тепла начинает испарять часть воды при постоянной температуре. В этой точке линия состояния начинает двигаться по диаграмме горизонтально вправо и на рисунке 2.15.4 представлена горизонтальной линией испарения, идущей от линии насыщенной воды к линии сухого насыщенного пара. Поскольку это процесс испарения, добавляемое тепло называется энтальпией испарения. Согласно паровым таблицам, при атмосферном давлении для испарения 1 kg воды в пар требуется 2256.71 kJ тепла. Поскольку это происходит при постоянной температуре 373.14 K, средняя температура на линии испарения также равна 373.14 K. Следовательно, изменение удельной энтропии от линии насыщенной воды до линии насыщенного пара составляет:
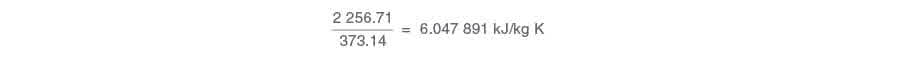
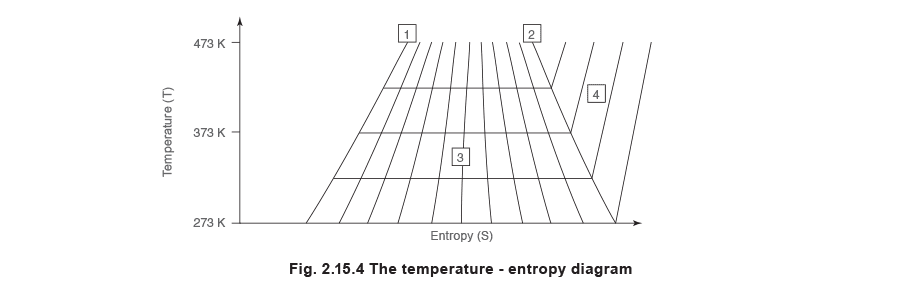
Полученная диаграмма температуры в зависимости от энтропии будет выглядеть примерно так, как на рисунке 2.15.4, где:
- 1 - линия насыщенной воды.
- 2 - линия сухого насыщенного пара.
- 3 - линии постоянной степени сухости в области влажного пара.
- 4 - линии постоянного давления в области перегрева.
Для чего используется диаграмма температура - энтропия (или T - S диаграмма)?
Для чего используется диаграмма температура - энтропия (или T - S диаграмма)?
Одно из возможных применений T - S диаграммы - отслеживание изменений состояния пара в процессах, где энтропия между начальным и конечным состоянием не меняется. Такие процессы называются изоэнтропическими, то есть происходящими при постоянной энтропии. К сожалению, линии постоянного теплосодержания на T - S диаграмме являются кривыми, что затрудняет отслеживание таких свободных и неограниченных расширений, как расширение пара после регулирующего клапана. В случае регулирующего клапана, где скорости в подводящем и отводящем трубопроводах примерно одинаковы, общий процесс происходит при постоянной энтальпии, то есть является изоэнтальпийным. В случае сопла, где конечная скорость остается высокой, процесс в целом происходит при постоянной энтропии. Чтобы отслеживать эти разные типы процессов, можно построить новую диаграмму с нанесенными давлениями и температурами, где по горизонтальной оси откладывается энтропия, а по вертикальной - энтальпия. Она называется диаграммой энтальпия - энтропия, или H - S диаграммой, см. рисунок 2.15.5.

H - S диаграмму также называют диаграммой Молье, в честь доктора Рихарда Молье из Дрездена, который впервые предложил такую форму диаграммы в 1904 году.
Теперь изоэнтальпийное расширение пара через регулирующий клапан можно просто представить прямой горизонтальной линией от начального состояния к конечному более низкому давлению справа на графике, см. рисунок 2.15.6; а изоэнтропическое расширение пара через сопло - линией, вертикально опускающейся от начального состояния к более низкому конечному давлению, см. рисунок 2.15.7.
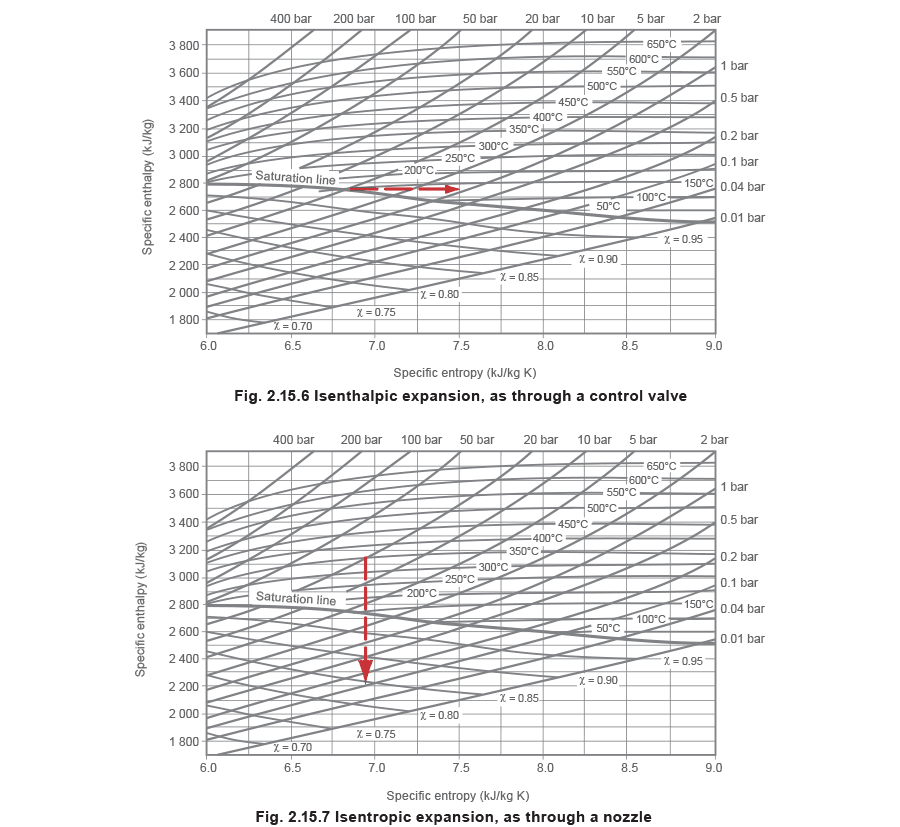
Изоэнтропическое расширение пара всегда сопровождается уменьшением энтальпии, и это называется "теплоперепадом" (H) между начальным и конечным состоянием. Значения H можно просто считать в начальной и конечной точках на диаграмме Молье, а их разность и дает теплоперепад. Точности диаграммы достаточно для большинства практических целей.
Интересно отметить, что поскольку расширение через отверстие регулирующего клапана является изоэнтальпийным процессом, обычно предполагают, что точка состояния перемещается прямо вправо, как показано на рисунке 2.15.6. На самом деле это не совсем так. Чтобы пройти через узкое сужение, пар должен разогнаться до более высокой скорости. Для этого он "заимствует" энергию из своей энтальпии и преобразует ее в кинетическую энергию. Это вызывает теплоперепад. Эта часть процесса является изоэнтропической, и точка состояния
перемещается вертикально вниз к более низкому давлению. После прохождения узкого сужения пар расширяется в область более низкого давления на выходе клапана и в конечном итоге замедляется по мере того, как объем корпуса клапана увеличивается и соединяется с downstream pipe. Это снижение скорости требует уменьшения кинетической энергии, которая в основном снова преобразуется в тепло и поглощается паром. Теплоперепад, вызвавший первоначальное увеличение кинетической энергии, восстанавливается, за исключением небольшой доли, теряемой из-за трения, и на H - S диаграмме точка состояния поднимается вверх по линии постоянного давления, пока не достигает того же значения энтальпии, что и в начальном состоянии. Траектория точки состояния показана на рисунке 2.15.8, где давление снижается с 5 bar при температуре насыщения до 1 bar, например, с помощью редукционного клапана. Энтальпия пара во входном состоянии при 5 bar составляет 2748 kJ/kg.
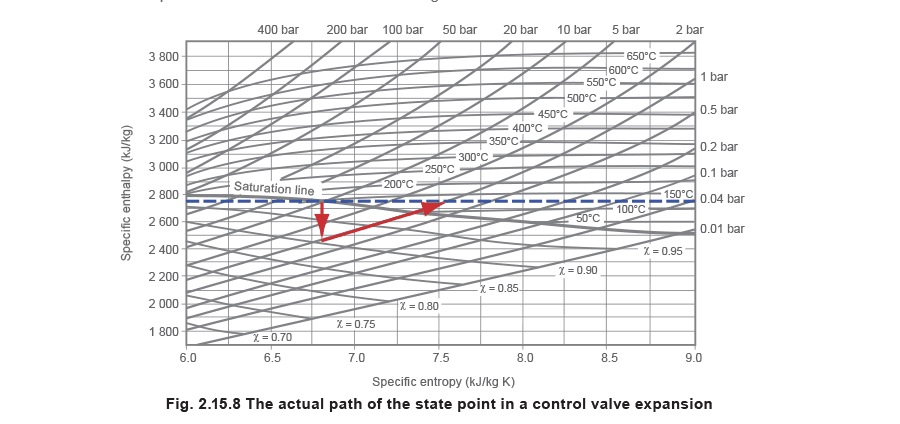
Интересно отметить, что в приведенном выше примере, показанном на рисунке 2.15.8, конечное состояние пара находится выше линии насыщения, а значит, пар является перегретым. Всякий раз, когда происходит такой процесс, обычно называемый дросселированием, конечное состояние пара в большинстве случаев оказывается суше, чем начальное. В результате получается либо более сухой насыщенный пар, либо перегретый пар, в зависимости от взаимного расположения начальной и конечной точек состояния.
Горизонтальное расстояние между начальной и конечной точками состояния представляет собой изменение энтропии. В этом примере, хотя общее изменение энтальпии отсутствовало, если пренебречь малыми потерями на трение, энтропия увеличилась примерно с 6.8 kJ/kg K до 7.6 kJ/kg K.
Энтропия в замкнутой системе всегда возрастает
Энтропия в замкнутой системе всегда возрастает
В любой замкнутой системе общее изменение энтропии всегда положительно, то есть энтропия всегда возрастает. Стоит рассмотреть это подробнее, поскольку именно здесь лежит основа самого понятия энтропии. Если энергия всегда сохраняется, как утверждает первый закон термодинамики, то есть не может быть создана или уничтожена, то того же нельзя сказать об энтропии. Второй закон термодинамики гласит, что всякий раз, когда энергия передается или преобразуется из одной формы
в другую, ее способность совершать работу уменьшается. В этом и состоит сущность энтропии.
Это мера недостатка потенциала или качества энергии; и после того как энергия была передана или преобразована, она уже не может вернуться к более высокому состоянию. Предельная истина состоит в том, что природа стремится к тому, чтобы все процессы во Вселенной в конечном итоге пришли к одной и той же температуре, поэтому энтропия Вселенной всегда возрастает. Пример 2.15.1 Рассмотрим чайник на кухонном столе, который только что был наполнен определенным количеством воды, содержащей 200 kJ тепловой энергии при 100 °C (373 K), из электрического чайника. Далее предположим, что температура воздуха вокруг кружки составляет 20 °C, а количество тепла в воде чайника в конце процесса будет равно 40 kJ. Второй закон термодинамики также утверждает, что тепло всегда переходит от более горячего тела к более холодному, и в этом примере очевидно, что если оставить чайник на достаточное время, он остынет до той же температуры, что и окружающий воздух.
Как изменятся значения энтропии для всего процесса?

Практические применения - теплообменники
Практические применения - теплообменники
В теплообменнике, где насыщенный пар на первичной стороне нагревает воду на вторичной стороне от 20 °C до 60 °C, пар будет конденсироваться по мере отдачи тепла. На диаграмме Молье это отображается смещением точки состояния влево от ее начального положения. В установившемся режиме сухой насыщенный пар конденсируется при постоянном давлении, и точка состояния пара перемещается вниз по линии постоянного давления, как показано на рисунке 2.15.9. Пример 2.15.2 В этом примере рассматривается конденсация пара из состояния насыщения при 2 bar и 120 °C с энтропией 7.13 kJ/kg K и энтальпией около 2700 kJ/kg. Видно, что точка состояния перемещается справа налево не горизонтально, а следуя по линии постоянного давления 2 bar. Диаграмма недостаточно велика, чтобы показать весь процесс конденсации, но если бы это было возможно, она показала бы, что конечная точка состояния пара расположилась бы при энтропии 1.53 kJ/kg K и энтальпии 504.8 kJ/kg, при 2 bar и 120 °C на линии насыщенной воды.
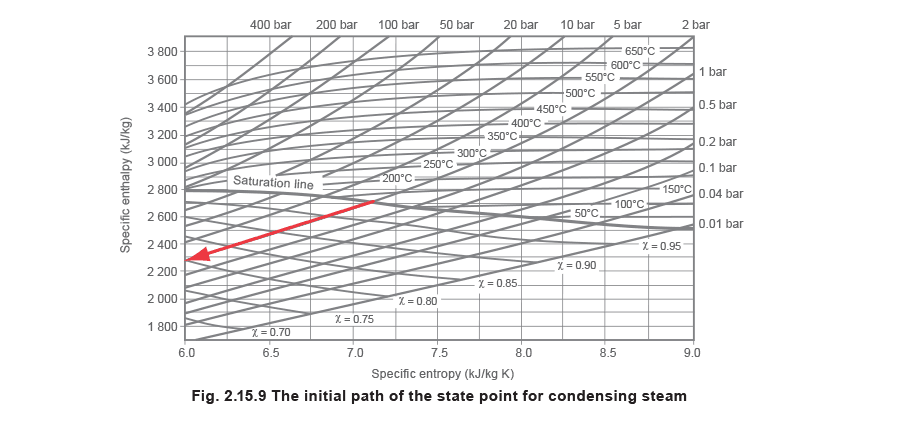
Из рисунка 2.15.9 видно, что при конденсации пара точка состояния опускается вниз по линии испарения, а энтропия уменьшается. Однако в любой общей системе энтропия должна увеличиваться, иначе был бы нарушен второй закон термодинамики. Как же тогда объяснить это уменьшение энтропии?
Как и в случае с чайником в примере 2.15.1, это уменьшение энтропии отражает лишь происходящее в одной части системы. Следует помнить, что любая полная система включает окружающую среду; в примере 2.15.2 это вода, которая получает тепло, передаваемое паром. В примере 2.15.2 вода получает ровно столько же тепла, сколько отдает пар, если считать, что потерь нет, но получает его при более низкой температуре, чем пар. Поскольку энтропия определяется как энтальпия, деленная на температуру, деление одного и того же количества тепла на более низкую температуру означает, что прирост энтропии воды будет больше, чем потери энтропии пара. Следовательно, в системе в целом наблюдается рост энтропии и общее рассеяние энергии.
Таблица 2.15.1 Относительная плотность / удельная теплоемкость различных твердых материалов
| Материал | Относительная плотность | Удельная теплоемкость kJ/kg °C |
| Aluminium | 2.55 - 2.80 | 0.92 |
| Andalusite | 0.71 | |
| Antimony | 0.2 | |
| Apatite | 0.83 | |
| Asbestos | 2.10 - 2.80 | 0.83 |
| Augite | 0.79 | |
| Bakelite, wood filler | 1.38 | |
| Bakelite, asbestos filler | 1.59 | |
| Barite | 4.5 | 0.46 |
| Barium | 3.5 | 2.93 |
| Basalt rock | 2.70 - 3.20 | 0.83 |
| Beryl | 0.83 | |
| Bismuth | 9.8 | 0.12 |
| Borax | 1.70 - 1.80 | 1 |
| Boron | 2.32 | 1.29 |
| Cadmium | 8.65 | 0.25 |
| Calcite, 0 - 37 °C | 0.79 | |
| Calcite, 0 - 100 °C | 0.83 | |
| Calcium | 4.58 | 0.62 |
| Carbon | 1.80 - 2.100 | 0.71 |
| Carborundum | 0.66 | |
| Cassiterite | 0.37 | |
| Cement, dry | 1.54 | |
| Cement, powder | 0.83 | |
| Charcoal | 1 | |
| Chalcopyrite | 0.54 | |
| Chromium | 7.1 | 0.5 |
| Clay | 1.80 - 2.60 | 0.92 |
| Coal | 0.64 - 0.93 | 1.08 - 1.54 |
| Cobalt | 8.9 | 0.46 |
| Concrete, stone | 0.79 | |
| Concrete, cinder | 0.75 | |
| Copper | 8.80 - 8.95 | 0.37 |
| Corundum | 0.41 | |
| Diamond | 3.51 | 0.62 |
| Dolomite rock | 2.9 | 0.92 |
| Fluorite | 0.92 | |
| Fluorspar | 0.87 | |
| Galena | 0.2 | |
| Proxylin plastics | 1.42 - 1.59 | |
| Quartz, 12.8 - 100 °C | 2.50 - 2.80 | 0.79 |
| Quartz, 0 °C | 0.71 | |
| Rock salt | 0.92 | |
| Rubber | 2 | |
| Sandstone | 2.00 - 2.60 | 0.92 |
| Serpentine | 2.70 - 2.80 | 1.08 |
| Silk | 1.38 | |
| Silver | 10.40 - 10.60 | 0.25 |
| Sodium | 0.97 | 1.25 |
| Steel | 7.8 | 0.5 |
| Stone | 0.83 | |
| Stoneware | 0.79 | |
| Talc | 2.60 - 2.80 | 0.87 |
| Tar | 1.2 | 1.46 |
| Tellurium | 6.00 - 6.24 | 0.2 |
| Tin | 7.20 - 7.50 | 0.2 |
| Tile, hollow | 0.62 | |
| Titanium | 4.5 | 0.58 |
| Topaz | 0.87 | |
| Tungsten | 19.22 | 0.16 |
| Vanadium | 5.96 | 0.5 |
| Vulcanite | 1.38 | |
| Wood | 0.35 - 0.99 | 1.33 - 2.00 |
| Wool | 1.32 | 1.38 |
| Zinc blend | 3.90 - 4.20 | 0.46 |
| Zinc | 6.90 - 7.20 | 0.37 |
Таблица 2.15.2 Относительная плотность / удельная теплоемкость различных жидкостей
| Жидкость | Относительная плотность | Удельная теплоемкость kJ/kg °C |
| Acetone | 0.79 | 2.13 |
| Alcohol, ethyl, 0 °C | 0.789 | 2.3 |
| Alcohol, ethyl, 40 °C | 0.789 | 2.72 |
| Alcohol, methyl, 4 - 10 °C | 0.796 | 2.46 |
| Alcohol, methyl, 15 - 21 °C | 0.796 | 2.51 |
| Ammonia 0 °C | 0.62 | 4.6 |
| Ammonia 40 °C | 4.85 | |
| Ammonia 80 °C | 5.39 | |
| Ammonia 100 °C | 6.19 | |
| Ammonia 114 °C | 6.73 | |
| Anilin | 1.02 | 2.17 |
| Benzol | 1.75 | |
| Calcium chloride | 1.2 | 3.05 |
| Castor oil | 1.79 | |
| Citron oil | 1.84 | |
| Diphenylamine | 1.16 | 1.92 |
| Ethyl ether | 2.21 | |
| Ethylene glycol | 2.21 | |
| Fuel oil | 0.96 | 1.67 |
| Fuel oil | 0.91 | 1.84 |
| Fuel oil | 0.86 | 1.88 |
| Fuel oil | 0.81 | 2.09 |
| Gasoline | 2.21 | |
| Glycerine | 1.26 | 2.42 |
| Kerosene | 2 | |
| Mercury | 19.6 | 1.38 |
| Naphthalene | 1.14 | 1.71 |
| Nitrobenzole | 1.5 | |
| Olive oil | 0.91 - 0.9400 | 1.96 |
| Petroleum | 2.13 | |
| Potassium hydrate | 1.24 | 3.68 |
| Жидкость | Относительная плотность | Удельная теплоемкость kJ/kg °C |
| Sea water | 1.0235 | 3.93 |
| Sesame oil | 1.63 | |
| Sodium chloride | 1.19 | 3.3 |
| Sodium hydrate | 1.27 | 3.93 |
| Soybean oil | 1.96 | |
| Toluol | 0.866 | 1.5 |
| Turpentine | 0.87 | 1.71 |
| Water | 1 | 4.18 |
| Xylene | 0.861 - 0.8810 | 1.71 |
Таблица 2.15.3 Удельная теплоемкость газов и паров
| Газ или пар | Удельная теплоемкость kJ/kg °C (при постоянном давлении) |
| Acetone | 1.31 |
| Air, dry, 0 °C | 1 |
| Air, dry, 100 °C | 1.01 |
| Air, dry, 200 °C | 1.03 |
| Air, dry, 300 °C | 1.05 |
| Air, dry, 400 °C | 1.07 |
| Air, dry, 500 °C | 1.09 |
| Alcohol, C2 H5 OH | 1.66 |
| Alcohol, CH3 OH | 1.53 |
| Ammonia | 1.76 |
| Argon | 0.3 |
| Benzene, C6 H6 | 0.98 |
| Bromine | 0.19 |
| Carbon dioxide | 0.62 |
| Carbon monoxide | 0.71 |
| Carbon disulphide | 0.55 |
| Chlorine | 3.43 |
| Chloroform | 0.54 |
| Ether | 1.95 |
| Hydrochloric acid | 0.56 |
| Hydrogen | 10 |
| Hydrogen sulphide | 0.79 |
| Methane | 1.86 |
| Nitrogen | 0.71 |
| Nitric oxide | 0.69 |
| Nitrogen tetroxide | 4.59 |
| Nitrous oxide | 0.69 |
| Oxygen | 0.65 |
| Steam, 0.5 bar a saturated | 1.99 |
| Steam, 2 bar a saturated | 2.13 |
| Steam, 10 bar a saturated | 2.56 |
| Steam, 0.5 bar a 150 °C | 1.95 |
| Steam, 2 bar a 200 °C | 2.01 |
| Steam, 10 bar a 250 °C | 2.21 |
| Sulphur dioxide | 0.49 |
